Production d'Entropie dans un Transfert Thermique Conductif
Contexte : Thermodynamique des Processus Irréversibles (TPI).
Dans cet exercice, nous allons étudier la création d'entropie lors d'un transfert de chaleur à travers une barre conductrice isolée latéralement. Ce phénomène est fondamental en Thermodynamique Hors ÉquilibreBranche de la thermodynamique étudiant les systèmes qui ne sont pas en équilibre global., car tout transfert thermique dû à une différence de température est un processus irréversible qui génère de l'EntropieMesure du désordre ou de la dégradation de l'énergie d'un système..
Remarque Pédagogique : Comprendre la source de l'irréversibilité est essentiel pour optimiser les processus énergétiques et comprendre le second principe sous sa forme locale.
Objectifs Pédagogiques
- Comprendre le lien entre flux de chaleur et production d'entropie.
- Calculer la production d'entropie globale dans un système stationnaire.
- Manipuler la relation de Gibbs locale.
Données de l'étude
On considère une barre cylindrique de longueur \(L\) et de section \(S\), parfaitement isolée sur ses faces latérales. Ses deux extrémités sont maintenues à des températures constantes \(T_1\) (source chaude) et \(T_2\) (source froide), avec \(T_1 > T_2\).
Fiche Technique / Données
| Caractéristique | Valeur |
|---|---|
| Matériau | Cuivre |
| RégimeÉtat du système (ici, les grandeurs ne dépendent pas du temps). | Stationnaire |
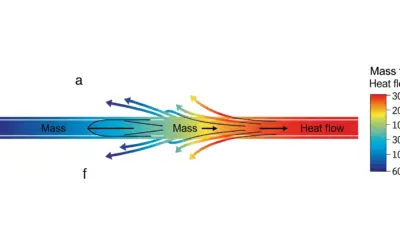
Schéma du Système Thermique
| Nom du Paramètre | Symbole | Valeur | Unité |
|---|---|---|---|
| Température Chaude | \(T_1\) | 400 | \(\text{K}\) |
| Température Froide | \(T_2\) | 300 | \(\text{K}\) |
| Flux de chaleur total | \(\dot{Q}\) | 500 | \(\text{W}\) |
Questions à traiter
- Rappeler l'expression du bilan d'entropie global pour un système ouvert.
- Simplifier ce bilan pour notre barre en régime stationnaire.
- Exprimer le flux d'entropie entrant et sortant.
- Calculer le taux de production d'entropie global \(\dot{S}_{\text{i}}\) (ou \(\sigma\)).
- Vérifier que ce taux est positif, conformément au second principe.
Les bases théoriques
La Thermodynamique des Processus IrréversiblesExtension de la thermo classique aux systèmes hors équilibre avec flux (chaleur, matière). (TPI) postule l'existence d'un équilibre thermodynamique local.
Bilan d'Entropie (Système Ouvert)
La variation d'entropie d'un système est la somme de l'entropie échangée avec l'extérieur et de l'entropie créée à l'intérieur.
Bilan global
Où :
- \(\dot{S}_{\text{e}}\) : Flux d'entropie échangé (dû aux transferts thermiques).
- \(\dot{S}_{\text{i}}\) : Production d'entropie interne (toujours \(\geq 0\)).
Flux d'Entropie Thermique
Pour un échange de chaleur \(\dot{Q}\) à une température \(T\) :
Définition
Second Principe (Forme Locale)
L'entropie ne peut être que créée, jamais détruite.
Inégalité fondamentale
Correction : Production d'Entropie dans un Transfert Thermique Conductif
Question 1 : Expression du Bilan d'Entropie Global
Principe
Pour tout système thermodynamique, la variation temporelle de l'entropie \(S\) est due à deux causes distinctes : les échanges avec l'extérieur et la création interne propre au système.
Mini-Cours
L'entropie est une grandeur extensive (elle s'additionne) mais non conservative : elle peut être créée mais jamais détruite. Contrairement à l'énergie qui se conserve, l'entropie a une "source" interne.
Remarque Pédagogique
Il est crucial de bien distinguer ce qui traverse la frontière (échange \(\dot{S}_{\text{e}}\)) de ce qui naît à l'intérieur du volume (création \(\dot{S}_{\text{i}}\)). Pour un système isolé, seul \(\dot{S}_{\text{i}}\) existe.
Normes
Selon la convention IUPAC et la norme ISO 80000-5, un flux reçu par le système est compté positivement.
Formule(s)
Bilan Général
Hypothèses
Ce bilan est valide pour tout système ouvert, quel que soit le régime (stationnaire ou transitoire), tant que l'hypothèse d'équilibre local est respectée.
Donnée(s)
| Variable | Signification | Unité |
|---|---|---|
| \(S_{\text{syst}}\) | Entropie totale du système | \(\text{J/K}\) |
| \(\dot{S}_{\text{i}}\) | Taux de production d'entropie | \(\text{W/K}\) |
| \(\dot{S}_{\text{e}}\) | Flux d'entropie échangé | \(\text{W/K}\) |
Astuces
Pensez à un compte en banque avec des frais : Variation Solde = Dépôts (Se) - Frais (Si négatif ? Non !). Ici c'est l'inverse : Si est toujours un gain (création), jamais une perte.
Schéma de Principe : Bilan Entropique
Calcul(s)
Interprétation
Il n'y a pas de calcul numérique ici, il s'agit d'établir le modèle théorique de base.
Schéma (Résultat)
Le schéma précédent illustre déjà la relation établie et reste valide.
Réflexions
Cette équation montre que l'entropie n'est pas conservée, contrairement à l'énergie interne U (où \(dU/dt = \dot{Q} + \dot{W}\) sans terme de création).
Points de vigilance
Ne confondez pas \(\dot{S}_{\text{e}}\) (échange aux frontières dû à la chaleur ou matière) et \(\dot{S}_{\text{i}}\) (génération volumique due aux irréversibilités).
Points à Retenir
L'équation fondamentale est : Variation = Échange + Production.
- Production \(\geq\) 0 (Second Principe)
- Échange peut être négatif (si on refroidit le système)
Le saviez-vous ?
Rudolf Clausius a introduit ce concept en 1865 en déclarant : "L'entropie de l'univers tend vers un maximum".
FAQ
Peut-on mesurer directement l'entropie ?
Non, on mesure ses variations indirectement via des échanges de chaleur (\(\delta Q\)) et de température (\(T\)), ou par calcul statistique.
A vous de jouer
Si le système est isolé (\(\dot{S}_{\text{e}} = 0\)), comment varie S ?
📝 Mémo
\(dS/dt = \text{Se} + \text{Si}\).
Question 2 : Simplification en Régime Stationnaire
Principe
Le régime StationnaireLes variables d'état ne dépendent pas du temps. implique que l'état thermodynamique macroscopique du système est constant dans le temps, même si des flux le traversent continuellement.
Mini-Cours
En régime permanent (steady-state), aucune grandeur extensive (\(T\), \(P\), \(S\), \(U\), \(m\)) ne s'accumule dans le volume de contrôle. La dérivée par rapport au temps est nulle.
Remarque Pédagogique
Stationnaire ne veut pas dire équilibre ! Des flux traversent le système et de l'entropie est créée, mais elle est évacuée aussitôt.
Normes
Hypothèse standard en génie des procédés pour les bilans continus (Flow process).
Formule(s)
Condition de stationnarité
Hypothèses
On suppose que le régime transitoire (mise en chauffe) est terminé et que les températures en tout point de la barre sont stabilisées.
Donnée(s)
| État | Dérivée temporelle |
|---|---|
| Stationnaire | \(\partial X / \partial t = 0\) |
Astuces
Si "régime permanent" ou "établi" est mentionné dans un énoncé, mettez immédiatement toutes les dérivées temporelles \(\partial/\partial t\) à zéro.
Schéma : Analogie Régime Permanent
Calcul(s)
La définition même du régime stationnaire impose que les grandeurs d'état locales ne varient plus dans le temps. Mathématiquement, cela se traduit par l'annulation de la dérivée temporelle :
Annulation du terme d'accumulation
En injectant ce résultat nul dans l'équation du bilan global établie à la Question 1, l'équation se simplifie considérablement :
Interprétation physique : Cette égalité montre un équilibre dynamique parfait. L'entropie créée à l'intérieur (\(\dot{S}_{\text{i}}\)) doit être intégralement compensée par un flux net d'entropie vers l'extérieur (\(- \dot{S}_{\text{e}}\)).
Schéma (Équilibre Flux/Création)
Réflexions
Cela signifie que le système évacue exactement autant d'entropie qu'il en produit. Il agit comme un "convertisseur" d'entropie vers l'extérieur pour maintenir son ordre interne.
Points de vigilance
Cela ne veut pas dire que \(\text{Si} = 0\) ! Cela veut dire que l'accumulation est nulle. L'entropie est produite, mais ne reste pas dans le système.
Points à Retenir
En régime permanent : Création = - Échange net.
Le saviez-vous ?
C'est exactement ce que fait la Terre ! Elle reçoit de l'énergie solaire (basse entropie) et réémet de l'infrarouge (haute entropie) pour ne pas "surchauffer" entropiquement.
FAQ
Et si Si n'est pas évacuée ?
L'entropie du système augmente (\(dS/dt > 0\)), sa température change, et on n'est plus en régime stationnaire.
A vous de jouer
Si \(\text{Si} > 0\), que doit valoir \(\text{Se}\) pour maintenir l'état ?
📝 Mémo
Tout ce qui est créé doit sortir.
Question 3 : Expression des Flux d'Entropie
Principe
L'entropie est transportée par la chaleur. Le flux d'entropie est défini par le rapport du flux thermique sur la température absolue à la frontière où l'échange a lieu.
Mini-Cours
Relation fondamentale : \(dS = \delta Q / T\). Le flux est donc \(\dot{S} = \dot{Q}/T\). Plus la température est basse, plus un même transfert de chaleur transporte d'entropie.
Remarque Pédagogique
La "qualité" de l'énergie thermique dépend de sa température. Diviser par \(T\) reflète cette qualité (ou dégradation).
Normes
Unités SI : Watts par Kelvin (\(\text{W/K}\)).
Formule(s)
Flux Entropique
Hypothèses
Les températures \(T_1\) et \(T_2\) sont uniformes sur les faces d'entrée et de sortie. La barre est isolée latéralement (adiabatique), donc \(Q\) est constant le long de la barre.
Donnée(s)
| Frontière | Température | Flux Chaleur |
|---|---|---|
| Entrée (Chaude) | \(T_1\) | \(+\dot{Q}\) |
| Sortie (Froide) | \(T_2\) | \(-\dot{Q}\) |
Astuces
Convention de signe : Tout ce qui entre est positif pour le système. \(Q\) entre en 1, donc \(Q_1 = +Q\). \(Q\) sort en 2, donc \(Q_2 = -Q\).
Détail des Flux aux Interfaces
Calcul(s)
Calculons d'abord les flux individuels :
Flux Entrant (Source T1)
À la frontière gauche, le système est en contact avec la source chaude \(T_1\). Il reçoit de la chaleur, ce qui augmente son entropie :
Le signe \((+)\) indique un gain pour le système.
Flux Sortant (Source T2)
À la frontière droite, le système est en contact avec la source froide \(T_2\). Il cède de la chaleur, ce qui diminue son entropie :
Le signe \((-)\) indique une perte pour le système.
Somme Algébrique
Le flux d'entropie total échangé \(\dot{S}_{\text{e}}\) est simplement la somme de ces deux contributions :
Pour simplifier l'expression finale, nous pouvons mettre le flux thermique \(\dot{Q}\) en facteur commun :
Schéma (Résultat)
Le flux net d'entropie est négatif car \(T_2 < T_1\), donc \(1/T_2 > 1/T_1\). Le terme sortant (négatif) est plus grand en valeur absolue que le terme entrant.
Réflexions
On constate que le système "perd" plus d'entropie en sortie qu'il n'en gagne en entrée via la chaleur. C'est nécessaire : il doit évacuer l'entropie reçue PLUS l'entropie qu'il a créée lui-même.
Points de vigilance
Ne pas inverser \(T_1\) et \(T_2\). Le terme sortant (négatif) a le plus petit dénominateur, donc la plus grande valeur absolue.
Points à Retenir
\(\text{Se} = \text{Entrée} - \text{Sortie}\). Ici \(\text{Se} < 0\).
Le saviez-vous ?
C'est le principe des machines thermiques : rejeter de la chaleur à basse température pour évacuer l'entropie accumulée lors du cycle.
FAQ
Pourquoi Q est le même en entrée et sortie ?
Car nous sommes en régime stationnaire et adiabatique latéralement : conservation de l'énergie (1er principe).
A vous de jouer
Si \(T_1=T_2\), que vaut le flux net ?
📝 Mémo
\(\text{Se}\) est négatif ici.
Question 4 : Calcul de la Production d'Entropie \(\dot{S}_{\text{i}}\)
Principe
Il ne reste plus qu'à combiner l'équation du bilan (Q2) et l'expression des flux (Q3) pour trouver la production interne.
Mini-Cours
Le calcul permet de quantifier l'irréversibilité du transfert. Plus \(\text{Si}\) est grand, plus on dégrade de l'énergie noble.
Remarque Pédagogique
C'est l'étape finale de la résolution du problème physique : relier la création d'entropie aux conditions aux limites.
Normes
Les résultats doivent être donnés avec les unités correctes (\(\text{W/K}\)) et un nombre cohérent de chiffres significatifs.
Formule(s)
On sait que \(\dot{S}_{\text{i}} = - \dot{S}_{\text{e}}\). Reprenons l'expression de \(\dot{S}_{\text{e}}\) trouvée précédemment :
En distribuant le signe moins dans la parenthèse, on inverse l'ordre des termes (\(-(A - B) = B - A\)) :
Hypothèses
Pas de nouvelle hypothèse, application directe.
Donnée(s)
| Variable | Valeur | Unité |
|---|---|---|
| \(\dot{Q}\) | 500 | \(\text{W}\) |
| \(T_1\) | 400 | \(\text{K}\) |
| \(T_2\) | 300 | \(\text{K}\) |
Astuces
Calculez d'abord les inverses des températures (\(1/T\)) ou mettez au même dénominateur (\(\frac{T_1-T_2}{T_1 T_2}\)) pour éviter les erreurs d'arrondi.
Application numérique directe des formules établies.
Calcul(s)
1. Calcul des inverses des températures
Commençons par évaluer les "affinités" entropiques, c'est-à-dire les inverses des températures absolues :
On observe que l'inverse de la température froide est plus grand que celui de la chaude.
2. Calcul de la différence (Gradient entropique)
Calculons maintenant la différence entre ces deux termes, qui représente la "force motrice" de la création d'entropie :
Pour une précision maximale, on peut aussi utiliser le calcul fractionnaire exact :
3. Multiplication par le flux thermique
Enfin, multiplions ce facteur géométrique et thermique par la puissance traversant le système (\(\dot{Q} = 500\) W) :
Ce qui nous donne la valeur décimale finale :
Schéma (Résultat)
La valeur positive est confirmée (\(0.417 > 0\)).
Réflexions
Cette valeur de \(0.417 \text{ W/K}\) représente le "coût entropique" du transfert de 500W entre ces deux températures. C'est l'entropie créée par seconde dans la barre.
Points de vigilance
N'oubliez pas l'unité \(\text{W/K}\) (et non \(\text{J/K}\) car c'est un débit temporel).
Points à Retenir
Plus l'écart de température est grand, plus la production est forte (pour un \(Q\) donné).
Le saviez-vous ?
En génie thermique, on cherche souvent à minimiser cette production pour améliorer le rendement (minimisation de la destruction d'exergie).
FAQ
Est-ce beaucoup ?
Cela dépend de la puissance mise en jeu. Pour 500W, c'est significatif. Pour un réacteur nucléaire, ce serait négligeable.
A vous de jouer
Que deviendrait la production d'entropie si on doublait le flux thermique \(\dot{Q}\) ?
📝 Mémo
\(\text{Si} > 0\).
Question 5 : Vérification du Second Principe
Principe
Le Second Principe de la thermodynamique stipule que pour tout processus réel (irréversible), la production d'entropie doit être strictement positive.
Mini-Cours
\(\dot{S}_{\text{i}} > 0\) : Irréversible (Réel).
\(\dot{S}_{\text{i}} = 0\) : Réversible (Idéal).
\(\dot{S}_{\text{i}} < 0\) : Impossible.
Remarque Pédagogique
C'est le critère ultime de validité physique d'un processus. Si vous trouvez \(\text{Si} < 0\), votre système viole les lois de la physique.
Normes
Postulat fondamental de la thermodynamique.
Formule(s)
Hypothèses
On vérifie si le transfert spontané du chaud (\(T_1\)) vers le froid (\(T_2\)) est possible.
Donnée(s)
| Condition | Valeur |
|---|---|
| Gradient | \(T_1 > T_2\) |
| Flux | \(\dot{Q} > 0\) |
Astuces
La fonction inverse \(f(x) = 1/x\) est décroissante. Si \(T_1 > T_2\), alors \(1/T_1 < 1/T_2\).
Analyse des signes mathématiques.
Calcul(s)
Analyse du Terme A
Puisque \(T_1 > T_2\) (\(400 > 300\)), on a \(\frac{1}{T_2} > \frac{1}{T_1}\). Le terme entre parenthèses est donc strictement positif.
Conclusion
Le produit d'un flux positif (\(\dot{Q}\)) par un terme positif est positif.
Schéma (Validation)
Réflexions
Le transfert thermique est bien un phénomène irréversible. On ne peut pas "dé-mélanger" le chaud et le froid spontanément sans travail extérieur.
Points de vigilance
Si vous aviez trouvé une valeur négative, cela signifierait soit une erreur de calcul (inversion \(T_1/T_2\)), soit que le processus décrit (transfert spontané du froid vers le chaud sans travail) est impossible (énoncé de Clausius) !
Points à Retenir
La chaleur coule spontanément vers les températures décroissantes, créant de l'entropie.
Le saviez-vous ?
Léon Brillouin a lié l'entropie à l'information (Néguentropie). Créer de l'information (ordre) coûte de l'énergie.
FAQ
Et pour une machine frigo ?
On force le transfert du froid vers le chaud en apportant du travail (\(W\)). L'entropie du système baisse peut-être localement, mais l'entropie globale (incluant la source d'énergie du travail) augmente.
A vous de jouer
Quelle loi physique impose ce signe ?
📝 Mémo
Irréversibilité validée.
Schéma Bilan des Flux d'Entropie
Visualisation des flux entrant et sortant et de la création interne.
📝 Grand Mémo : TPI et Transfert Thermique
Ce qu'il faut retenir pour les examens :
-
🔥
Source de l'irréversibilité : C'est la différence de température (gradient \(\nabla T\)) qui génère l'entropie.
-
⚖️
Stationnaire \(\neq\) Équilibre : En régime stationnaire, le système ne change pas, mais il produit continuellement de l'entropie qu'il évacue.
-
📐
Formule Clé : \(\dot{S}_{\text{i}} = \dot{Q} \left( \frac{1}{T_{\text{froid}}} - \frac{1}{T_{\text{chaud}}} \right)\).
🎛️ Simulateur : Impact du Gradient de Température
Modifiez les températures et le flux pour observer l'évolution de la production d'entropie.
Paramètres
📝 Quiz final : Maîtrisez-vous la TPI ?
1. Dans un système isolé, comment évolue l'entropie lors d'un processus irréversible ?
2. Si T1 = T2 (équilibre thermique), que vaut la production d'entropie ?
3. Quelle est l'unité de la production d'entropie par unité de temps ?
📚 Glossaire
- Entropie (S)
- Fonction d'état extensive mesurant le degré de désordre d'un système. Unité : J/K.
- Flux Thermique (Q)
- Quantité d'énergie thermique transférée par unité de temps. Unité : Watt (W).
- Irréversibilité
- Caractéristique d'un processus qui ne peut être inversé sans apport d'énergie extérieur, entraînant une création d'entropie.
- Régime Stationnaire
- État où les variables macroscopiques en tout point du système sont constantes dans le temps.
- Source de Chaleur
- Réservoir thermique dont la capacité calorifique est suffisante pour que sa température reste constante malgré les échanges.
Le Saviez-vous ?
Chargement...



0 commentaires